Avaliação da Anvisa e Fim da Patente da Semaglutida
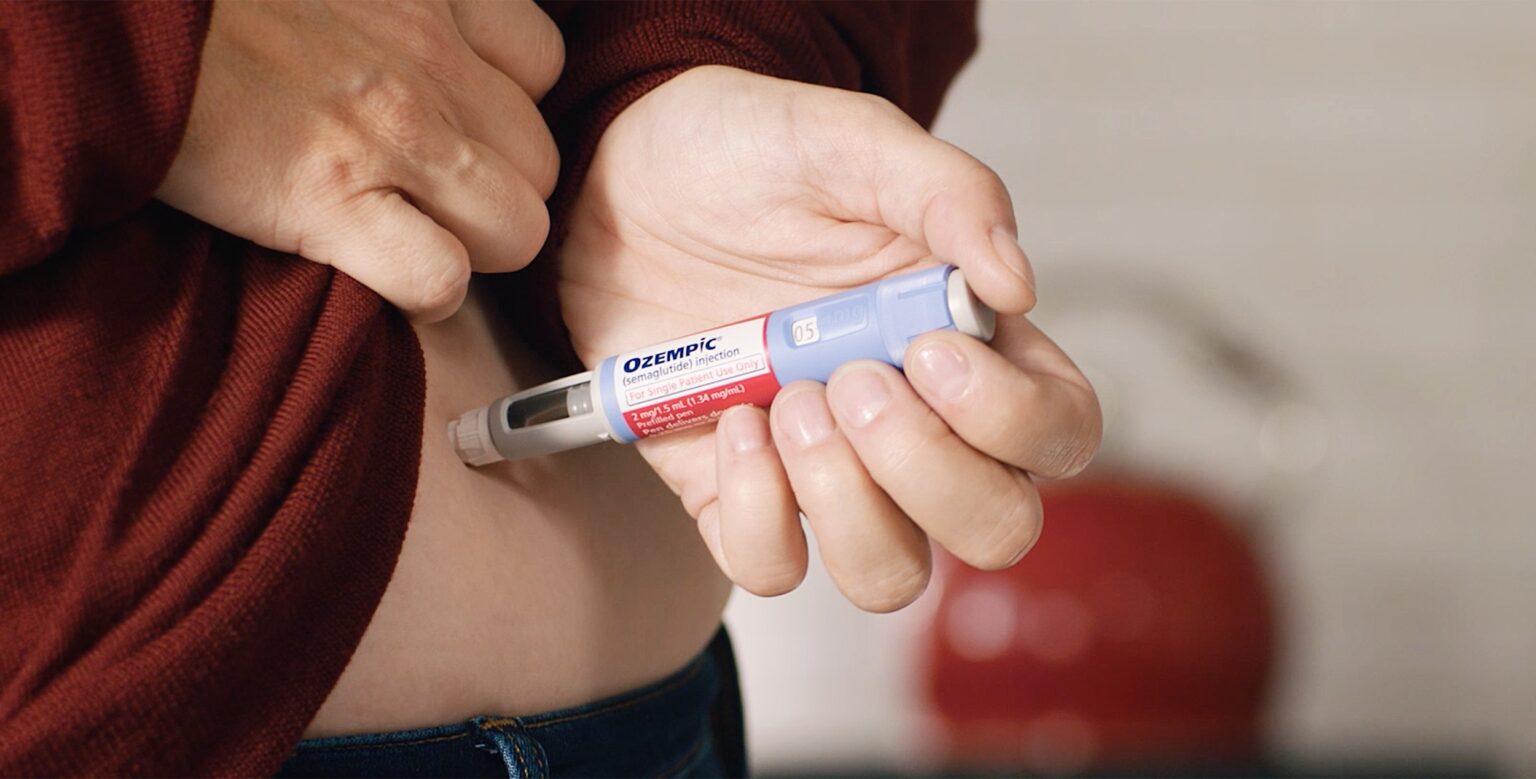
A Agência Nacional de Vigilância Sanitária (Anvisa) está prestes a tomar uma decisão crucial na próxima semana sobre a aprovação de versões nacionais do Ozempic, medicamento à base de semaglutida. Com a patente da substância, desenvolvida pela farmacêutica dinamarquesa Novo Nordisk, prestes a expirar em 20 de março, outras empresas poderão desenvolver e comercializar produtos similares no Brasil, desde que obtenham as devidas aprovações regulatórias.
No ano anterior, o Ministério da Saúde havia solicitado que a Anvisa priorizasse a análise de canetas injetáveis produzidas nacionalmente. Agora, os resultados desse pedido começam a se materializar, com uma expectativa de decisão que pode impactar o mercado em breve. Contudo, é importante destacar que a aprovação não é garantida e a Anvisa pode exigir informações adicionais às farmacêuticas antes de conceder o aval definitivo.
Impacto no Mercado e Expectativas de Redução de Preços
Especialistas do setor avaliam que, com a entrada de novas versões nacionais no mercado, a expectativa é de que os preços dos medicamentos para tratamento da obesidade possam cair. Essa redução, no entanto, deve ocorrer gradualmente, impulsionada pela concorrência entre as empresas. A EMS, um dos laboratórios que está se preparando para esse cenário, já anunciou que possui a infraestrutura necessária para a produção de canetas injetáveis dessa classe, mas ainda não definiu um cronograma para lançamento ou detalhes sobre a política de preços de seus produtos. Segundo a empresa, qualquer avanço nesse sentido depende exclusivamente do cumprimento das etapas regulatórias.
Vale lembrar que a EMS já é conhecida por ter lançado canetas injetáveis para emagrecimento de uma geração anterior de medicamentos, que utilizam a liraglutida como princípio ativo. Com isso, a empresa demonstra sua experiência nesse mercado e sua disposição para entrar na nova fase que se abre com a possibilidade de versões de semaglutida.